我国多中心研究证实靶向 IL-6R 治疗视神经脊髓炎谱系疾病的有效性
《柳叶刀-神经病学》(The Lancet Neurology,影响因子IF=28.755)于2020年4月22日在线发表由天津医科大学总医院和北京天坛医院神经内科施福东教授牵头、全国六家医院参与完成的大型随机对照临床试验结果。该试验报道IL-6R阻断剂托珠单抗(Tocilizumab)较传统的免疫抑制剂硫唑嘌呤(Azathioprine),在降低视神经脊髓炎谱系疾病(neuromyelitis optica spectrum disorder,NMOSD)患者的复发率和致残率上具有明显优势,为该疾病的治疗提供了高级(I级)循证医学证据。文章“Safety and efficacy of tocilizumab versus azathioprine in highly relapsing neuromyelitis optica spectrum disorder (TANGO): an open-label, multicentre, randomised, phase 2 trial”。
NMOSD是一种高复发、高致残性的中枢神经系统自身免疫性疾病,以反复发生的视神经炎和脊髓炎为主要特征。该病自2004年被确立为独立的疾病以来,尚无预防复发的免疫疗法的指南。在目前,我国对NMOSD的治疗和世界上其他国家相似,主要以经典的免疫抑制剂如硫唑嘌呤、吗替麦考酚酯等和CD20单抗利妥昔单抗治疗为主。即使应用上述药物,但仍有25-50%的患者在随访期间出现疾病的复发。每次复发会导致疾病残疾的累积,患者的神经系统功能无法恢复到复发前的水平。2019年,先后有三个国外的多中心随机对照试验的结果提示,与安慰剂相比,补体抑制剂依库珠单抗(Eculizumab)、CD19单抗Inebilizumab、IL-6R单抗Satralizumab均可显著降低NMOSD复发的风险。其中,Eculizumab已被美国食药品监督管理局批准用于治疗NMOSD。新的靶向药物和经典的免疫抑制剂相比,长期治疗的安全性和疗效性如何,目前在全球范围内尚无对比性的临床研究。为解决上述问题,施福东教授团队基于NMOSD发病机制的探索,首次开展靶向IL-6R的另一种药物托珠单抗,与硫唑嘌呤相比,治疗NMOSD的头对头对比性临床研究(简称为TANGO试验)。托珠单抗是人源化IL-6受体(IL-6R)的单克隆抗体,可抑制促IL-6信号通路,阻止外周B细胞异常活化,在NMOSD患者中的疗效亟待证实。硫唑嘌呤是一种抑制嘌呤核苷酸生物合成的免疫抑制药,是目前作为治疗NMOSD的一线药物之一,但具有致白细胞降低和肝功能异常等副作用。
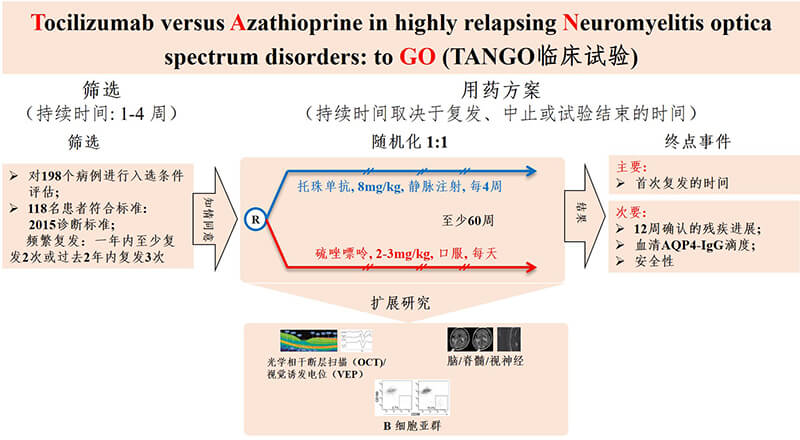
图1. TANGO试验方案(ClinicalTrials. gov. number: NCT03350633)
自2017年11月至2018年8月,TANGO试验招募了118例临床高度复发的确诊为NMOSD患者,其中约40%的患者合并其它自身免疫性疾病。这些患者在随机前1年至少有2次复发,或者随机前2年至少有3次复发。所有患者按照1:1的比例随机分为托珠单抗组和硫唑嘌呤组,每组59例。托珠单抗组患者接受8mg/kg/m的静脉点滴治疗,硫唑嘌呤患者接受2-3mg/kg/d的口服治疗。两种疗法分别经过12周和24周的洗脱期后,患者均接受单药治疗方案。主要终点事件是自用药开始后的复发情况 (图1)。与硫唑嘌呤相比,托珠单抗显著延长了从随机化开始到疾病复发之间的时间间隔 (托珠单抗组中位数78.9周 vs 硫唑嘌呤组中位数56.7周,P=0.0026)。至临床试验结束时,托珠单抗组仅有8例患者复发,而硫唑嘌呤组有28例复发。相比硫唑嘌呤,托珠单抗显著降低了76.4%的复发风险(hazard ratio [HR]=0.236, 95% confidence interval [CI]: 0.107-0.518; P<0·0001) (图2)。在单药治疗阶段,托珠单抗组和硫唑嘌呤组分别有6例和23例复发,托珠单抗降低了81.2%的复发风险(HR=0.188, 95% CI: 0.076-0.463; P<0.0001)。与硫唑嘌呤相比,托珠单抗组患者出现12周疾病残疾进展的比例显著降低 (HR=0.288, 95% CI: 0.105-0.795; P=0.0087),外周血水通道蛋白4自身抗体(AQP4-IgG)的滴度下降50%,而硫唑嘌呤组血清AQP4-IgG的滴度在整个治疗期间没有明显变化。将患者是否合并其它自身免疫性疾病进行分层分析发现,无论患者是否合并其它自身免疫性疾病,托珠单抗亦均明显地比硫唑嘌呤降低了复发风险 (图3)。从安全性上来看,托珠单抗与硫唑嘌呤的副作用发生率基本相当,大多数不良反应为轻至中度,如上呼吸道感染、肝功能异常等。但托珠单抗组出现药物治疗相关的副作用的比例(61%)低于硫唑嘌呤组(83%)。
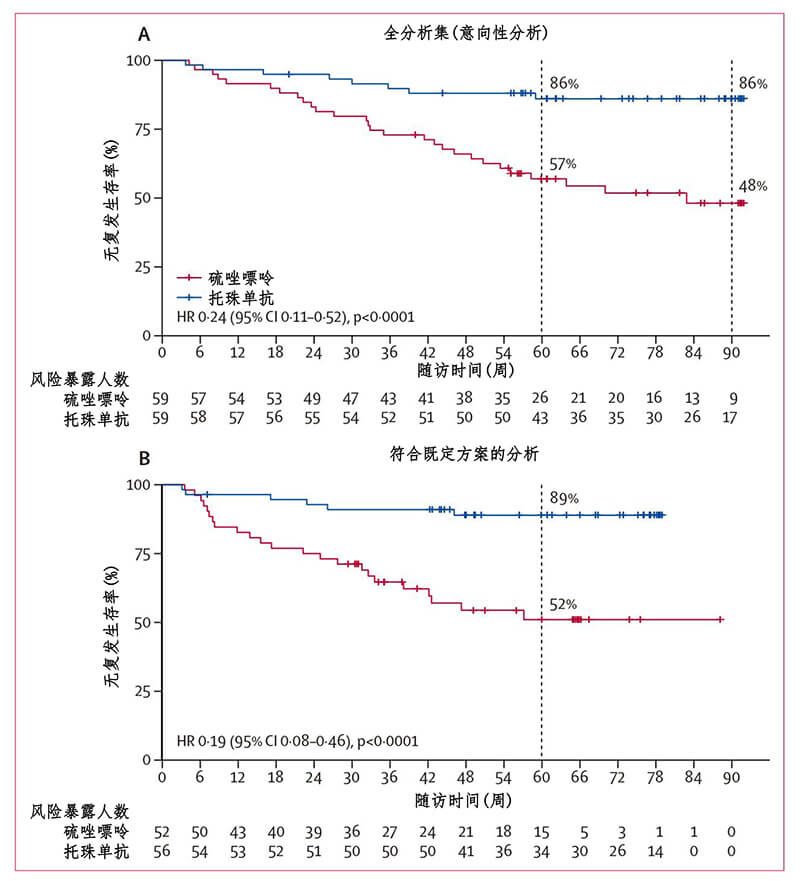
图2. TANGO试验主要终点事件(自随机化开始的NMOSD复发情况)
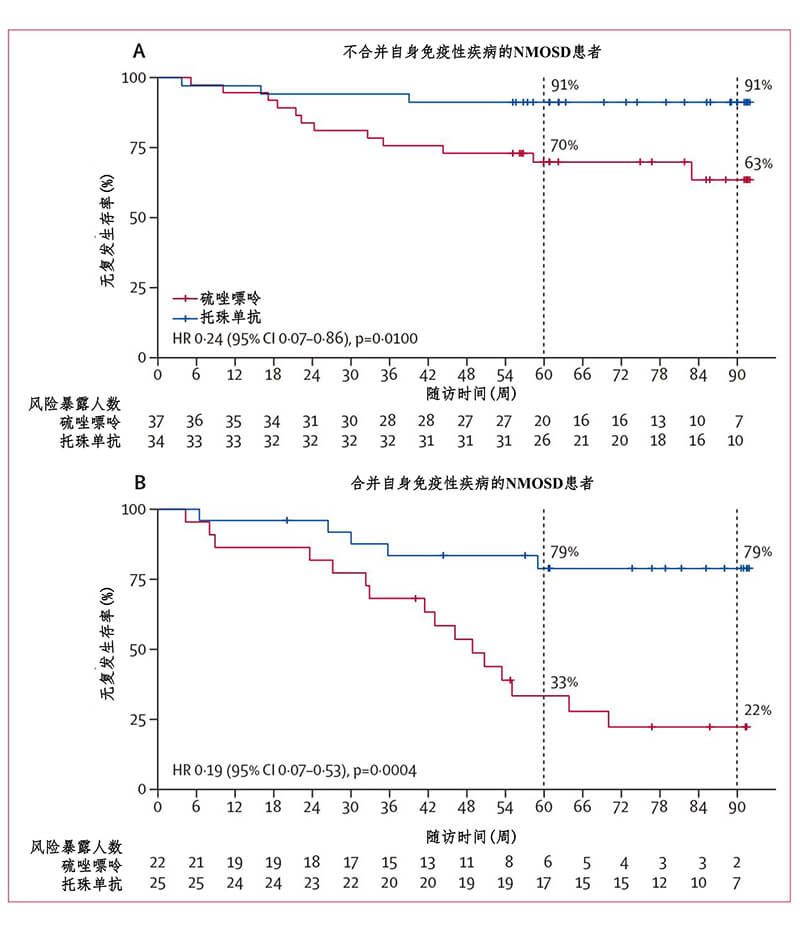
图3. 按照NMOSD患者是否合并其它自身免疫性疾病对复发情况进行分层分析(全分析集)
TANGO试验的主要结果提示,与硫唑嘌呤相比,靶向IL-6R的托珠单抗可显著降低NMOSD复发的风险,对于复发率较高或难治性NMOSD患者,尤其是合并自身免疫性疾病的患者,托珠单抗可作为NMOSD的首选。为NMOSD患者提供了新的安全有效的治疗方案。TANGO试验将极大地促进靶向IL-6R疗法会进入NMOSD的国际诊疗指南,指导全球神经科医生如何选择新的靶向治疗和传统的免疫抑制剂。
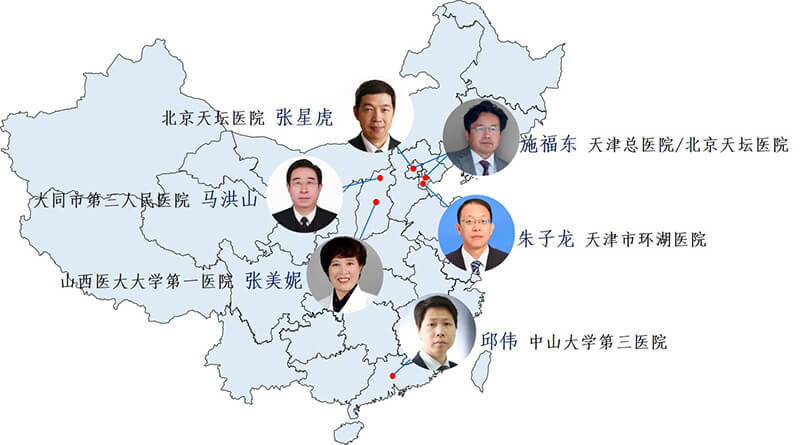
图4. TANGO试验中心和区域PI分布
TANGO试验是一个研究者自主设计、自筹经费、独立于任何制药公司、全球首个头对头对比性的随机对照研究,由全国六家医院的资深专家合作完成(图4)。在为期两年的临床试验期间,论文第一作者张超医生在6家医院之间数次往复监察、协调,保证临床试验的高质量和多中心试验的一致性,而且他代表TANGO试验的研究团队在国际大会上公布研究成果(图5),得到国际同行的广泛认可和支持。

图5. 论文第一作者张超医生在第35届欧洲多发性硬化治疗与研究大会(ECTRIMS)上代表TANGO试验研究者做大会主题报告(瑞典,斯德哥尔摩,2019.9.12)
TANGO试验的设计和实施均严格采取国际标准。不同于前述三个临床试验,TANGO试验的患者的纳入标准根据2015年最新的基于国际专家共识的NMOSD诊断标准。除了经典的终点事件(如临床复发、残疾进展等),TANGO试验还采用客观的视觉评价,如视觉诱发电位(VEP)和光学相干断层成像(OCT)以及核磁共振影像学(MRI)指标对病灶和脑和脊髓容量进行评价。更为重要的是,TANGO试验采用转染细胞免疫荧光法(CBA法)对患者血清的水通道蛋白4 (Aquaporin 4, AQP4)自身抗体进行定量检测。该方法由京津神经免疫中心和天津天海新域生物科技有限公司的严格质控,可动态了解药物治疗期间该致病性自身抗体的变化,为评价药物的疗效提供了直接依据,同时为今后NMOSD 患者的诊断、病情监控和临床试验奠定了成熟的,国际认可的方法学基础。
TANGO试验是施福东教授团队近10年以来在靶向B细胞治疗多发性硬化、视神经脊髓炎谱系疾病、重症肌无力等疾病方面的深度探索。自2010年开始,该团队建立了低剂量的抗CD20单抗利妥昔单抗序贯补充治疗方法,通过流式细胞术监测删除B细胞后的效果,有效控制了视神经脊髓炎谱系疾病的复发,同时极大地降低了患者的年治疗费用(Neurology 2013)。该治疗方案被中国、韩国和日本等多个神经病学中心采用,使越来越多的患者受益。针对部分利妥昔单抗治疗效果欠佳的患者,张超医生作为主要研究者引入蛋白酶体抑制剂硼替佐米作为附加疗法,通过删除产生病理性抗体的浆细胞控制难治性患者的疾病复发(JAMA Neurology, 2017)。而托珠单抗不会删除B细胞或浆细胞,而是通过抑制自身反应性B细胞的活性,使患者达到免疫平衡的状态(图6)。目前该团队正在利用单细胞测序和多组学等技术对外周血和脑脊液中的B细胞进行深入研究,试图全面阐明B细胞在NMOSD中的作用机制,为开展更精准靶向B细胞的治疗方案奠定理论基础。
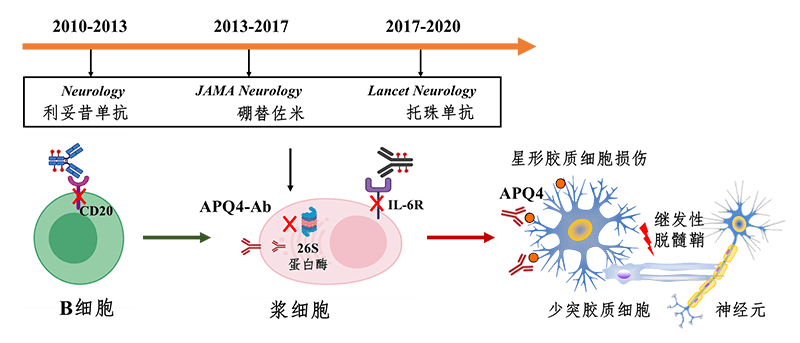
图6. 京津神经免疫团队靶向细胞NMOSD疗法探索——10年之旅
TANGO试验为NMOSD患者提供了科学系统地预防疾病复发的全新理念,是我国神经免疫领域合作的结晶,展现了我国在全球神经免疫领域中的临床研究水平。此外,TANGO试验在《The Lancet Neurology》的修稿,正值我国新型冠状病毒疾病(COVID-19)疫情严重期间,文章最后高度赞誉了来自天津总医院,北京天坛医院和全国医务人员在抗击新型冠状病毒疾病过程中的无私奉献和自我牺牲的精神。
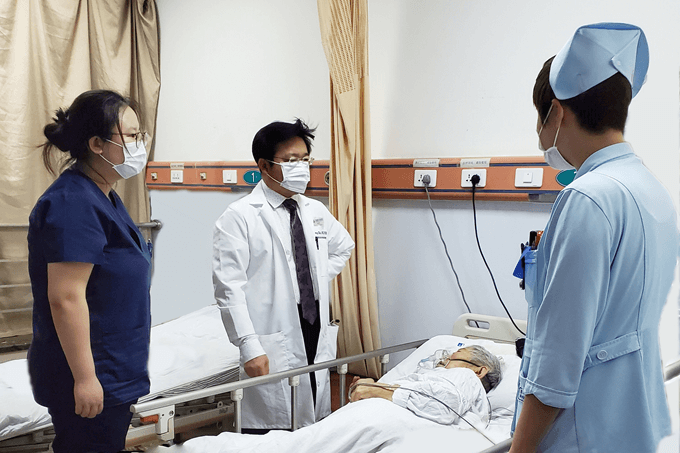
图7. 施福东教授(中)在2020年1月23日查看一名发热的视神经脊髓炎患者
TANGO试验主要研究者简介
施福东教授 主任医师,天津医科大学总医院、北京天坛医院、京津神经免疫中心 (图7)
瑞典Karolinska学院神经病学博士,擅长神经免疫疾病,包括多发性硬化,视神经脊髓炎,重症肌无力等疾病的诊断、治疗和研究。施福东分别在哈尔滨医科大学,北京协和医院,瑞典Karolinska学院,美国Scripps研究院,美国Barrow神经病学研究所先后完成临床和科研训练。为“长江学者”特聘教授、国家重大科学研究计划项目(973)首席科学家, 泛亚多发性硬化治疗和研究(PACTRIMS)学术委员会主席, 中华医学会神经病学分会神经免疫学组组长, 担任Science Translational Medicine编委。全球最大出版商Elsevier独立分析显示,过去五年施福东在神经炎症相关领域的科技产出名列全球第20位,引用率为全球第5位,H指数41。
参考文献
- Zhang C, Zhang M, Qiu W, Zhang X, Ma H, Zhu Z, Yang CS, Jia D, Zhang TX, Yuan M, Feng Y, Yang L, Lu W, Yu C, Bennett J, Shi FD. Safety and efficacy of tocilizumab versus azathioprine in highly relapsing neuromyelitis optica spectrum disorder (TANGO): an open-label, multicentre, randomised, phase 2 trial. Lancet Neurology 2020; 19: 391-401.
- Zhang C, Tian DC, Yang CS, Han B, Wang J, Yang L, Shi FD. Safety and efficacy of bortezomib in patients with highly relapsing neuromyelitis optica spectrum disorder. JAMA Neurol, 2017, 74(8):1010-12.
- Yang CS, Yang L, Li T, Zhang DQ, Jin WN, Li MS, Su N, Zhangning N, Liu Q, Shao ZH, Yu C, Shi FD, Responsiveness to reduced dosage of rituximab in Chinese patients with neuromyelitis optica. Neurology, 2013, 81(8):710-3.


